日本东京工业大学荣誉教授大隅良典获得今年诺贝尔生理学或医学奖后,其研究成果“自噬作用”相关机制备受瞩目,当时研究人员发现细胞能够消灭自身内部物质,方式是将其包裹进一个膜结构中,从而形成小型囊体并被输运至被称作溶酶体(lysosomes)的回收机构进行分解,这种小型整体被称为自噬体(autophagosome)。
在肝脏的各种损伤中,自噬发挥了双重作用,自噬体的研究是其重要的表现方式。最近几年,一种叫做外泌体(exosome)的小囊泡正受到大家广泛的关注。肝癌细胞exosome所含肿瘤抗原和免疫分子,可以体外大规模制备抗肝癌亚细胞瘤苗。人体细胞内含有各种直径、功能各不相同的“囊泡”,在各自的岗位上发挥着自己的作用,囊泡各类繁多,容易混淆,在此,本文对常见的几种“囊泡”做一简单汇总,供大家实验参考。
1. 自噬体(autophagosome)
自噬(autophagy)是由Ashford和Porter在1962年发现细胞内有"自己吃自己"的现象后提出的,是指从粗面内质网的无核糖体附着区脱落的双层膜包裹部分胞质和细胞内需降解的细胞器、蛋白质等成分形成自噬体(autophagosome),
大小:直径一般为300~900 nm,平均500 nm,
内涵:其囊泡内常见的包含物有胞质成分和某些细胞器如线粒体、内吞体、过氧化物酶体等。
功能:与溶酶体融合形成自噬溶酶体,降解其所包裹的内容物,以实现细胞本身的代谢需要和某些细胞器的更新。
特点:在机体的生理和病理过程中都能见到;与其他细胞器相比,自噬体的半衰期很短,只有8 min左右,说明自噬是细胞对于环境变化的有效反应。
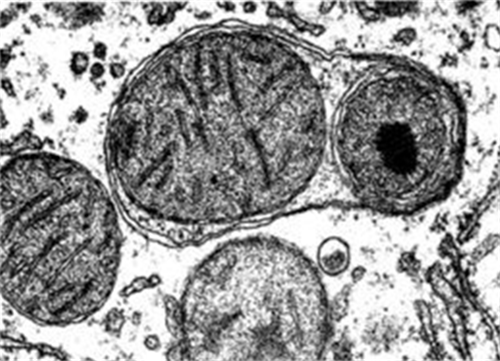
2. 溶酶体(lysosomes)
真核细胞中的一种细胞器;为单层膜包被的囊状结构,对酸性磷酸酶的活性为阳性,专司分解各种外源和内源的大分子物质。
大小:由6~8nm米厚的单层膜所围着的,大小(在电镜下显示多为球形,但存在橄球形,故不能说直径)约25~800纳米,平均为400纳米的颗粒或小泡。
内涵:内含多种水解酶,根据内含物和形成阶段的不同,溶酶体可分为两大类,具有均质基质的颗粒状溶酶体称为初级溶酶体(primary lysosome),含有复杂的髓磷脂样结构的液泡状溶酶体称为次级溶酶体(secondary lysosome)。初级溶酶体虽含有水解酶,但是它是未进行消化作用的溶酶体。次级溶酶体(消化泡)是由初级溶酶体与细胞吞噬作用所产生的吞噬体相互融合而成的,并且是已供给水解酶的溶酶体。在次级溶酶体中含有摄食的物质,并对其进行消化。根据底物的来源,又可分为异噬溶酶体(phagolysosome)和自噬溶酶体(autophagolysosome),前者消化的物质来自外源,后者消化的物质来自细胞本身的各种组分。
功能:与自噬体融合后,形成自噬溶酶体,消化分解内源性物质;与吞噬体结合吞噬溶酶体,将大分子物质分解成简单物质;与异吞噬体结合,形成异噬溶酶体,分解外源性物质。吞噬溶酶体和自噬溶酶体将物质水解成小分子物质,被细胞吸收,还残留一些不被消化和吸收的物质称为残质小体(residual body)。
3. 自噬溶酶体(autolysosome)
自噬体与溶酶体融合后,形成自噬溶酶体。自噬性溶酶体是一种自体吞噬泡,作用底物是内源性的,即细胞内的蜕变、破损的某些细胞器或局部细胞质。
形态:它们由单层膜包围,内部常含有尚未分解的内质网、线粒体和高尔基复合体或脂类、糖原等。
功能:正常细胞中的自噬性溶酶体在消化、分解、自然更替一些细胞内的结构上起着重要作用。这种溶酶体广泛存在于正常的细胞内,在细胞内起"清道夫"作用,作为细胞内细胞器和其它结构自然减员和更新的正常途径。当细胞受到药物作用、射线照射和机械损伤等各种理化因素伤害时时,其数量明显地增多,因此对细胞的损伤起一种保护作用。
在介绍以下几种小体时,首先介绍一下胞吞作用。胞吞作用可分为吞噬作用、胞饮作用以及受体介导的胞吞作用。吞噬作用(phagocy-tosis)为各种变形的、具有吞噬能力的细胞所特有,吞噬的物质多为颗粒性的,如微生物、组织掉片和异物等,在胞内形成吞噬小体。胞饮作用(Pinocytosis)由质膜包裹液态物质形成吞饮小泡或吞饮体的过程,形成吞饮小体;受体介导的胞吞作用,在质膜上形成凹陷,当特定大分子与凹陷部位的相应受体结合时,凹陷进一步向胞质回缩,并从质膜上箍断形成有被小泡(coated vesicles),即胞内体(内体)。此后的过程就与内吞小泡进行的过程相同,这种受体介导内吞具有高度选择性,转运速度很快。

4. 吞噬小体(phagosome):
吞噬体也称为吞噬小体,是一种在胞吞作用中在被吞噬物质周围形成的囊泡,这种囊泡由细胞膜向细胞内凹陷产生。
大小:吞噬作用是以大的囊泡形式(常称为液泡)内吞较大的固体颗粒,可以吞噬直径达几微米的复合物、微生物以及细胞碎片。
作用:吞噬体是一种在免疫过程中常见的细胞结构,入侵机体的病原微生物可在吞噬体中被杀灭、消化。在成熟过程中吞噬体需与溶酶体融合,生成兼具隔离与分解异己物质能力的吞噬溶酶体,这种经两种囊泡融合而成的新囊泡只曾在动物细胞中发现。
5. 吞饮小体(pinosome)
胞饮过程中以小的囊泡形式将细胞周围的微滴状液体,吞入细胞内过程中形成的小体。
大小:直径一般小于1微米,常含有离子或小分子。
作用:吞饮小体与初级溶酶体接触时,双方接触部分的膜溶解,当各自的内容物互相混合,初级溶酶体内的酶就可以把所吞噬的外源性物质消化分解。
6. 胞内体(endosome)=内体:
动物细胞内由膜包围的细胞器,是转运由胞吞作用新摄取的物质到溶酶体被降解。胞内体被认为是胞吞物质的主要分选站。
大小:一个成熟的内体直径大约500纳米。内体是膜包裹的囊泡结构,有初级内体(early endosome)和次级内体(late endosome)之分,初级内体通常位于细胞质的外侧,次级内体常位于细胞质的内侧,靠近细胞核。
功能:胞内体被认为是膜泡运输的主要分选站之一。内体提供了细胞外物质进入细胞内的运载途径。例如很多病毒以此条途径进入细胞,以登革热病毒为例:病毒先吸附在细胞膜上,其后内体像袋子一样裹住病毒,病毒膜与内体膜融合,进入细胞质基质。再例如:低密度脂蛋白(LDL)进入细胞前,先与细胞表面的低密度脂蛋白受体结合。在到达初级前体时,胞内体膜上有ATP驱动的质子泵,将氢离子泵进胞内体腔中,使腔内的pH降低(pH5~6),从而引起低密度脂蛋白(LDL)与受体分离。含有低密度脂蛋白(LDL)的胞内体与溶酶体融合,低密度脂蛋白(LDL)被水解,释放出胆固醇和脂肪酸供细胞重复利用。
特点:内体的主要特征是酸性的、不含溶酶体酶的小囊泡,其内的受体与配体是分开的。一般认为初级内体是由于细胞的内吞作用而形成的含有内吞物质的膜结合的细胞器,通常是管状和小泡状的网络结构集合体。
次级内体中的pH呈酸性,且具有分拣作用,能够分选与配体结合的受体,让它们再循环到细胞质膜表面或高尔基体反面网络,次级内体中的受体和配体不再偶联在一起,所以次级内体又被称为CURL(compartment of uncoupling of receptor and ligand),意思是受体与配体非偶联的区室。
有学者将与溶酶体酶运输小泡融合的次级内体称为前溶酶体,因为此时的次级内体中有前体酶的存在。内体膜上具有ATPase-H+质子泵,利用H+质子的浓度,保证了内部pH的酸性。初级内体和次级内体是可以区别的,因为它们的密度、pH和酶的含量不相同。

7. 外泌体(exosome)
外泌体是细胞主动向胞外分泌的大小均一的囊泡样小体,具有抗肿瘤免疫、促血管新生等生理功能。不同类型的细胞可以释放出外泌体,正常生理状态下血液、尿液、乳汁和支气管灌洗液中也能分离到外泌体。1983年,外泌体首次于绵羊网织红细胞中被发现,1987年Johnstone将其命名为“exosome”。多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。
大小:现今,其特指直径在40-100nm的盘状囊泡。
功能:外泌体可以携带蛋白,运送RNA,在细胞间物质和信息转导中起重要作用。外泌体可能通过调控免疫功能,促进肿瘤血管新生和肿瘤转移,以及直接作用于肿瘤细胞等途径,影响肿瘤的进展。外泌体可应用于肿瘤的诊断。
有生物活性的外泌体合成开始于多泡体与质膜的融合,然后释放腔内囊泡作为外泌体,从树突细胞产生的外泌体(DEXOs)包含能够激活自然杀伤细胞(NK Cell)的配体。负载DEXOs的肿瘤抗原能够激活的肿瘤抗原的特异CD8阳性标记癌细胞毒性的T淋巴细胞(CTLs),因此能在动物模型和人类临床试验中诱导抗肿瘤反应。
在尿液中也能检测到外泌体,它们可以作为诊断工具反馈前列腺癌的治疗效果。因为来源于肿瘤细胞外泌体可以显示出调节肌纤维细胞的分化程度,也有调查显示,外泌体释放增多也与卵巢癌侵袭有关。

以上是对各种小体的简单介绍,希望各位科研人员在实验中理清思路、避免混淆。
(刘辉)
|

